EXERCICE I
En O un point de l’espace, on lance avec une vitesse V=20 m/s et suivant la verticale ascendante, un point matériel A. Le vecteur accélération de son mouvement est celui de la pesanteur de norme G= 10 m/s
- Etablir l’équation horaire du mouvement de A
- A quelle date A parvient-il à son altitude maximale ?
- Détermine cette altitude maximale
-
- D’après le départ de A on lance dans les mêmes conditions un second point B.
- A quelle date et à quelle altitude la rencontre A et B se produit ?
- Calculer les vitesses de A et B juste avant la rencontre et interpréter les résultats obtenus
- Tracer les diagrammes des espaces de A et B dans un même repère.
EXERCICE II
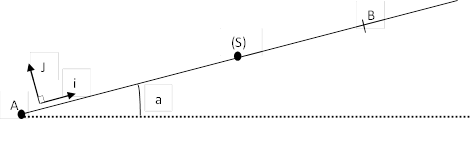
On lance suivant le plan incliné de a, un solide ponctuel(s) à partir de A avec une vitesse Vo, celui-ci soumis à des frottements de résultante constante f s’arrête en B puis redescend.
-
- Etablir l’expression de l’accélération a1 du solide lors de la monté
- Quelle est la nature de son mouvement ?
- En déduire son accélération a2 en descente et la nature du mouvement.
- On donne a1= -3,5 m/s2 a2= -2,5m/s2 AB=1,5; m= 200g
- Déterminer les valeurs de x et F
- Calculer la variation de l’énergie cinétique de (s) lors de ce déplacement. g= 10 m/s2
EXERCICE III
Dans les conditions où le volume molaire est de 251/mol on traite une masse m = 250 mg d’une amine saturé pour en libérer l’azote sous forme de diazote de volume 70 ml
- Déterminer en mole la quantité de matière en diazote libéré.
- En déduire dans cette masse d’amine, le pourcentage d’azote puis la formule brute de cette amine.
- Donner les formules semi-développées possibles de cette amine
- Lors de la réaction de l’amine avec le chlorure de méthyle ou chlorométhance, on obtient la triméthylamine.
- Quel caractère de l’amine cette réaction met-elle en évidence ?
- Quel atome est responsable de ce caractère.
- Déduire la formule et le nom de l’amine de départ.
EXERCICE IV
Un composé organique A a une formule brute CxHyO ; son oxydation ménagée conduit à un composé organique de formule C4H8O
- Donner les natures possibles de X
- En déduire les formules semi-développées possibles et le nom de A.
- Le composé (X) réagit avec la solution oxydante de bichromate de potassium et
donne l’acide 2-méthylpropanoïque. -
- Donner la formule puis le nom de l’acide 2-méthylpropanïque.
- Donner alors le nom et la formule de :
- ( X)
- A
- Ecrire l'équation bilan de la réaction entre ( X ) et la solution de dichromate de potassium

